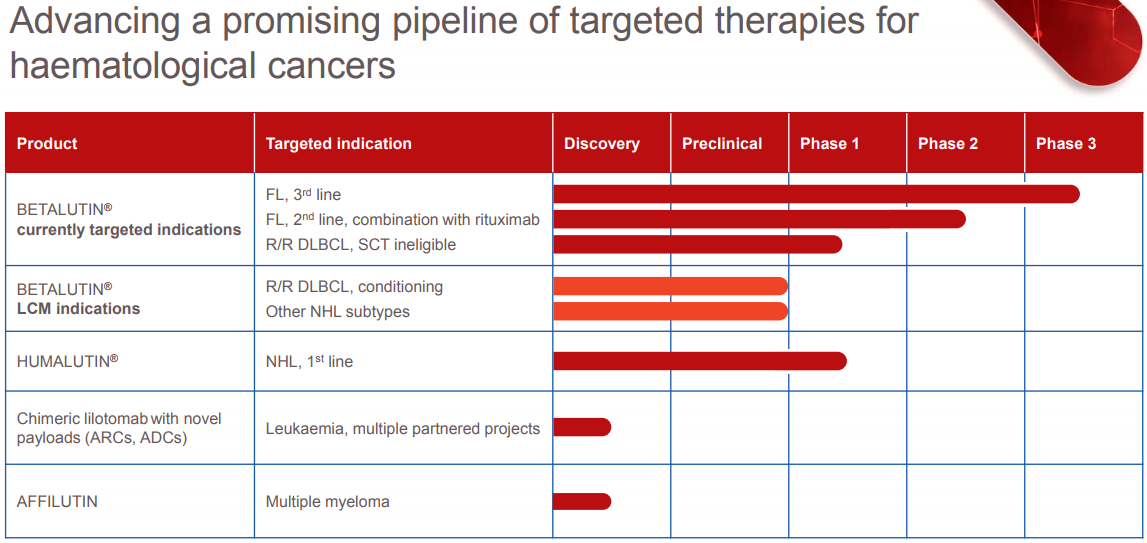
Hva er planene til Nordic Nanovector de neste årene?
Jeg har alt for lite å gjøre om dagen og bruker derfor en del tid på å fundere på investeringene mine, og kanskje i hovedsak den investeringen jeg har mest tro på i både det korte og lange bildet. Under har jeg skrevet hva jeg ser for meg skjer med kombinasjonsstudien de neste to årene.
Først: hvor er vi nå?
- Pivotal fase 2 for tredje linje FL
- Fase 1 i DLBCL, 2. dosenivå av 3
- Fase 1b for andre linje FL / kombinasjon med rituximab
Hva var planen, og hva er planen?
På Capital Markets Day i 2015 fortalte NANO ganske utfyllende om hva strategien var for å få Betalutin ut på markedet. Kort fortalt så skulle de kjøre en pivotalstudie i 3L og sende inn NDA(søknad) for godkjennelse. Men samtidig som denne søknaden blir sendt har de forpliktet seg til å kjøre en stor randomisert fase 3 andrelinje-studie.
Og vi vet hva det er de planlegger for andre linje. Betalutin + Rituximab.
Er det noen grunner til at denne strategien med “phase 3 second line study ongoing at filing” skal være forandret? Alt har jo blitt forskjøvet parallelt (bortsett fra det som har blitt lagt på is  )
)
Når jeg hører Lisa på Q2 fortelle at safetydata fra Archer -1 kommer til å bli med på labelen for Betalutin, er jeg overbevist om at oppstarten av Archer - 1 er i tide for å få initiert en stor randomisert fase 3 studie med betalutin og rituximab 2H20, samtidig Paradigmeresultatene blir sendt til FDA.
TImeline kan bli som følger.
- FPD Oktober 2018.
- 1 pasient i måneden til 3 pasienter har fått 10MBq.
- 3 måneders safety readout gir eskalering til 15MBq i mars 2019. Utvidelse til flere sites øker inkluderingshastigheten og de kan få inn 2 pasienter i måneden.
- mars til april, mai t.o.m juli: 3 pasienter med 15MBq, 3mnd safetyreadout.
- august - februar på 14 pasienter med 15 Mbq.
- mars - desember på analyse av studie og safety samt skriving av protokoll og søknader om fase 3 randomisert studie med Betalutin og Rituximab for andre linje follicular lymphoma.
Med denne timelinen kan de rekke å ha startet (ikke dosert) en fase 3-studie i 2FL i 2H20, samtidig som søknad om markedsføringtillatelse er sendt til FDA & EMA for 3FL.
God helg 
EDIT : Vil bare presisere at grunnen til at Archer - 1 er en fase 1b i stedet for fase 2 som opprinnelig tenkt, er at det er en First In Man-studie (kilde:Lisa R). I kraft av primært endepunkt sikkerhet og toleranse, og sekundærendepunkt tumorkontroll og varighet av tumorkontroll, er dette “også” en fase 1/2-studie.
EDIT 2: Legger til ett annet punkt som jeg mener peker mot at min teori kan være på riktig spor. På REK sine sider for 2018/727 står det
- Prosjektstart: 30.03.2018
- Prosjektslutt: 30.03.2025
5 års oppfølging etter siste pasient i mars 2020 vil gi prosjektslutt rundt da.