Hæ? Nei, jeg bare tiltrådte din egen konklusjon: listene er lunefulle og lite/ikke egnet til å kjøpe/selge på. At det er særlig mange som gjør det tror jeg ikke, i alle fall ikke etter «lærdommen» fra da aksjen dumpet 10 prosent på det som etter alle solemerker var ingenting. Og den har til gode å hente seg inn, uten at det er særlig overraskende heller.
Hehe beklager da las jeg svaret ditt på feil måte. Men ja, enig i at de listene og rekkefølge i de er uforutsigbare og ikke noe man kan ta som fasit.
Takk for deling! Ikke noe nytt her, alt går knirkefritt!
Elles blir det spennende om selskapet starter tilbakekjøp av aksjer? Vi får følge med underQ presentasjon.
Man kan trøste seg med at det ikke er kun i Skandinavia vi ikke skjønner 100% hvordan de listene fungerer. Ser ikke ut som de på kina forum skjønner det heller.
Her er en som har sin egen konklusjon 
“The key is that 1702 is not developed by the company, but bought other people’s patents. It seems that 1706 has been aborted by itself. That fake foreigner is mourning for money. The suspension of the review is likely to involve patent issues.”
Dine indlæg kan ikke siges mere rigtigt  — fuld kaos og frustration
— fuld kaos og frustration 
Dansken
Ja, hvis den dagen kommer skal jeg feire til de grader, vær så sikker. Når PHO er historie skal jeg aldri mer investere i biotek, ikke en eneste krone 
Bare et lite lodd i Oncoinvent 🫣
Den viktigste lærdommen er vel å ikke ta langsiktig posisjon på tidlig stadium i denne sektoren?
Dog kan man sige her, at PHO vel næppe er på et tidligt stadium, selv om Cevira ej endnu er endelig klar til at komme ud på markedet,
Ellers har det vist sig at - sell on news og genkøb senere, har vist sig at være langt mere indbringende i mange tilfælde i denne branche, end det bare at være langsigtet, UDEN disse handler.
Selvsagt med en vis risiko for at ramme skævt, men lader man den evt. gevinst/tab blive i banken og kun genkøber for det samme beløb man solgte for, er ovenstående påstand ikke helt uden en gram af sandhed.
DOG - ikke sige dette videre til nogen 
Nei, selvsagt ikke. Kommentaren var rettet til de som nå gleder seg til endelig å komme seg ut av dette selskapet. Flertallet av dem har nok vært investert i selskapet i mange år.
Det ser vel egentlig ut som man må være forberedt til å vente til neste år før vi får en forløsende melding? Dette om de kommer til å bruke opp til 30 dager før de publiserer avgjørelsen etter at alle lamper er slukket?
Idag er den plass 354… Så virker noe random de plasseringene der gitt. Om de ikke er på jobb idag og ja.
Vanskelig å forstå denne behandlingsprosedyren for godkjenning. Jeg innbilte meg at beskjeden om tilleggsopplysninger kun medførte en mindre behandlingsprosedyre kun knyttet til de elementer som var omfavnet av disse tilleggsopplysninger. I stedet virker det som om de foretar en full rebehandling av alle sider av Cevira?
Det tror jeg ikke er hva som skjer nå. En annen ting vi må være klar over er at Asieris er pliktig til å melde om det er noen “out of bounds” som skjer ang søknader. Akkurat som de gjorde ved beskjed om å sende inn tilleggsinformasjon.
Så hadde det vært noe lignende som skjedde denne gangen ved pausing så er de nok pliktig til å sende ut melding. Jeg ser de og henviser til det i sine svar på spørsmål rundt det med pause.
Synes bare det er underlig at det å sjekke ut tilleggsopplysningene skal ta minst like lang tid som det de brukte på hele Cevira fram til i vår.
Om man skal se på de 60 arbeidsdagene som har blitt nevnt tidligere som det kan se ut som er regelen, da er vi vel på ca den 3 november hvor den skal være ute av køen (har trekt ifra en uke som de hadde fri, Golden week)
Så sånn sett så er ting on target da om det stemmer med 60d etter innsendt tilleggsinfo.
Vi får håpe det virkelig er en regel, og ikke kun en målsetting. Holder 3/11, kan vi få avgjørelsen publisert senest i begynnelsen av desember.
Men nå får det være slutt med nytteløs spekulasjon fra min side i dag! Man blir gjerne litt rar og ensporet i hode, om man sitter for lenge og studerer maling som tørker… 
Ser med spenning frem til Q3!
Diskuterte litt med AI for å bli litt klokere på veien videre nå når Cevira er pauset. Kort oppsummert ønsket jeg å finne ut vanlige grunner til pausing, og fikk dette til svar (komprimert versjon):
| Possible Cause | Meaning | Implication |
|---|---|---|
| Supplemental data requested and awaiting submission | CDE has asked for additional CMC (pharmacy) or device data; review clock stops until the sponsor submits | Common and not negative; review resumes once data received |
| Awaiting coordination between divisions | One department (e.g. pharmacy/device) must finalize before others can conclude | Administrative — not a rejection |
| Device component or GMP verification pending | The CDE may need inspection or device conformity verification before completing review | Common for drug–device combination products |
| Temporary CDE workload reallocation | Administrative pause while CDE reorganizes internal review order | Neutral |
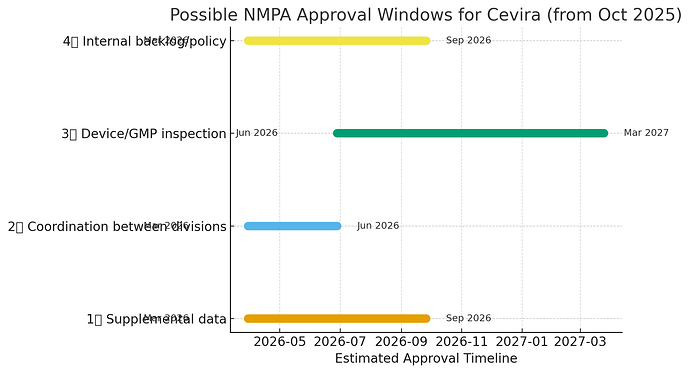
Jeg spurte så hva som var forventet timeline for hvert av scenarioene og fikk følgende oppsummering:
| Scenario | Likely Cause | Typical Pause | Total to Approval | Estimated Approval Window |
|---|---|---|---|---|
 Supplemental data requested Supplemental data requested |
Waiting on Asieris submission | 1–3 mo | 6–12 mo | Q2–Q4 2026 |
 Coordination between divisions Coordination between divisions |
Internal sync of reviews | 2–4 mo | 6–9 mo | Mid 2026 |
 Device or GMP inspection Device or GMP inspection |
Awaiting inspection/verification | 4–8 mo | 9–18 mo | Late 2026 – Mid 2027 |
 Internal CDE backlog/policy Internal CDE backlog/policy |
Administrative hold | 2–6 mo | 6–12 mo | Mid- – Late 2026 |
I følge AI er scenario 1 eller 3 mest sannsynlig årsak til pausing.
“In combination products like Cevira , the device component and drug CMC can complicate the review — device safety documentation sometimes falls under a separate technical group, and that can stall CMC progress even if clinical review is nearly done.”
Dette gir:
Out of interest, i ditt første spørsmål til AI, spurte du spesifikt ang pausing etter innsendt suplimented info, eller bare generelt pause under en søknad?
Om ikke så kan du kanskje prøve å spørre samme spørsmål, men inkludere “second round of review”?
Hadde vært interesant å se om de utgjør noe forskjell på svaret den gir da.
Hehe jeg er uenig med AI på hvilke punkt som ser mest sannsynlig ut og. Jeg tenkte 2 eller 4 som de mest sannsynlige. (mest nummer 2)
Skrev følgende:
“Cevira (APL-1702) has now reached the second round of technical review. Under «clinical» they have reached 4th place in the nmpa list. «Pharmacy» is on 359th place. All other light bulbs are gone. Now, it says «paused» under review status. How should this be interpreted?”
Jeg er forsåvidt enig i at pkt 2 er relevant, men føler den henger sammen med pkt 1. Hvorfor har vi så vidt sett fremgang på pharmacy? Jeg tipper Clinical ikke er forsvunnet fordi den avhenger av Pharmacy og at Pharmacy drøyer pga komplisert review eller behov for mer info.